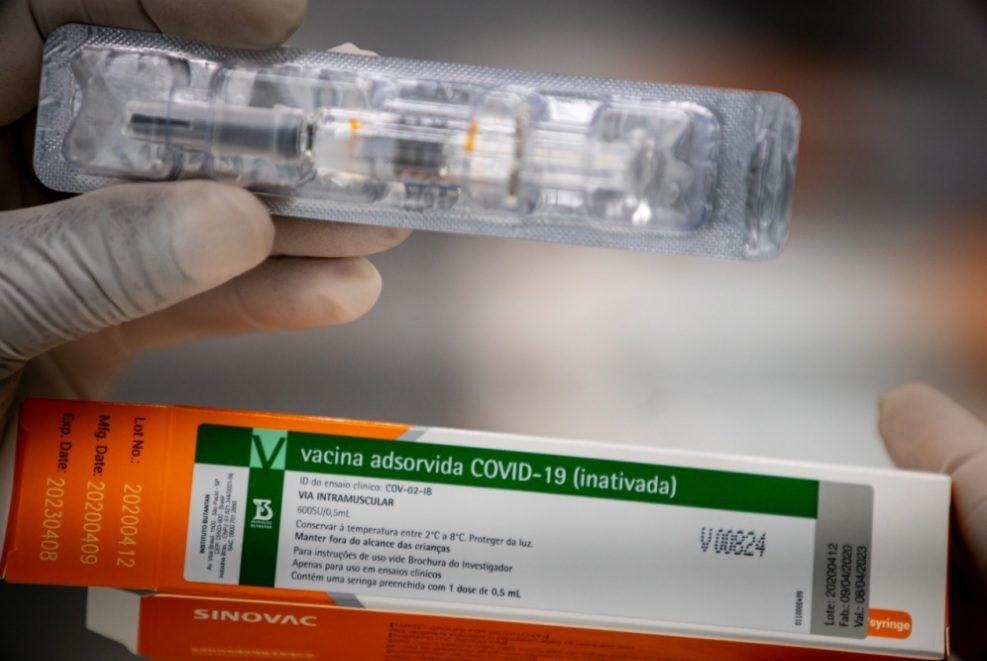
Dimas Covas, diretor do Instituto Butantan, afirmou que a CoronaVac pode estar disponível para a população em janeiro de 2021. A vacina contra o coronavírus é produzida em parceria pelo Butantan e pelo laboratório chinês SinoVac.
“A vacina estará disponível e o registro na Anvisa, acredito eu, também estará disponível. Então, poderemos iniciar um programa em janeiro, acredito, de vacinação. E espero [que] com o apoio do Ministério [da Saúde], apesar de todas essas declarações que não citam nominalmente a vacina do Butantan”, disse Dimas Covas em entrevista à GloboNews nesta quinta-feira, 3.
O diretor do Instituto Butantan ainda afirmou que espera que a CoronaVac seja incorporada ao plano de vacinação do governo federal. Na última terça-feira, 1º, o ministério da Saúde divulgou uma estratégia inicial para vacinar a população.
Segundo Dimas Covas, a vacina está perto de ser aprovada pela Agência Nacional de Vigilância Sanitária. “Nós estamos muito próximos de solicitar o registro. Nós não teremos a necessidade de solicitar esse registro emergencial, vamos solicitar já o registro da vacina. Estamos muito próximos de que isso aconteça. O registro e a vacina estando disponíveis, nós temos que iniciar a vacinação. É tudo o que nós queremos”, relatou.
A CoronaVac está na na terceira e última fase de testes. O governo de São Paulo tem um acordo para que sejam entregues 46 milhões de doses e para que a tecnologia seja transferida para o estado. Dessa forma, São Paulo poderá ter produção própria de imunização.
Em outubro, o ministro da Saúde, Eduardo Pazuello, havia anunciado que o governo federal compraria a vacina produzida pelo Instituto Butantan. No entanto, foi desautorizado pelo presidente Jair Bolsonaro (sem partido).
Houve ainda uma confusão entre Anvisa e Instituto Butantan, quando a agência interrompeu os testes da CoronaVac por causa da morte de um dos voluntários. Depois, descobriram que a morte não teve relação com a imunização e houve um suposto conflito na comunicação.
Na última quarta-feira, 2, a Anvisa afirmou que aceitará que empresas desenvolvedoras de vacinas peçam “uso de urgência”.